Zur Charakterisierung von Säuren in Lebensmitteln werden zwei Messgrößen verwendet, der pH-Wert und der Säuregrad, welche üblicherweise in wässrigen Lösungen ermittelt werden. Der pH-Wert ist ein Maß für die Stärke einer Säure, er beschreibt die dissoziierten (freiliegenden) Wasserstoffionen (H+). Der Säuregrad hingegen, bezeichnet die Menge einer Säure und beschreibt sowohl die dissoziierten, als auch die undissoziierten (gebundenen) Wasserstoffionen. In Abbildung 8.1 ist exemplarisch dargestellt, welche Wasserstoffionen von Essigsäure (CH3COOH) zur Bestimmung von pH-Wert und Säuregrad erfasst werden.
Zur Bestimmung des pH-Wertes werden 10 g eines Sauerteiges oder einer Brotkrume mit
5 ml Aceton und ca. 40 ml von insgesamt 100 ml destilliertem Wasser in einer Reibschale zu einem homogenen Brei verrührt. Der Brei wird dann mit den restlichen 60 ml in ein Becherglas überführt. Mit der Messelektrode eines pH-Wert-Messgerätes kann nun der pH-Wert in der wässrigen Lösung bestimmt werden. Soll zusätzlich der Säuregrad gemessen werden, wird die wässrige Lösung so lange mit Natronlauge (0,1 mol/l) titriert, bis ein pH-Wert von 8,5 erreicht ist. Der Verbrauch an Natronlauge (0,1 mol/l) in ml/10 g Probe, welcher notwendig ist, um die Säure in der wässrigen Lösung zu neutralisieren, entspricht dem Säuregrad
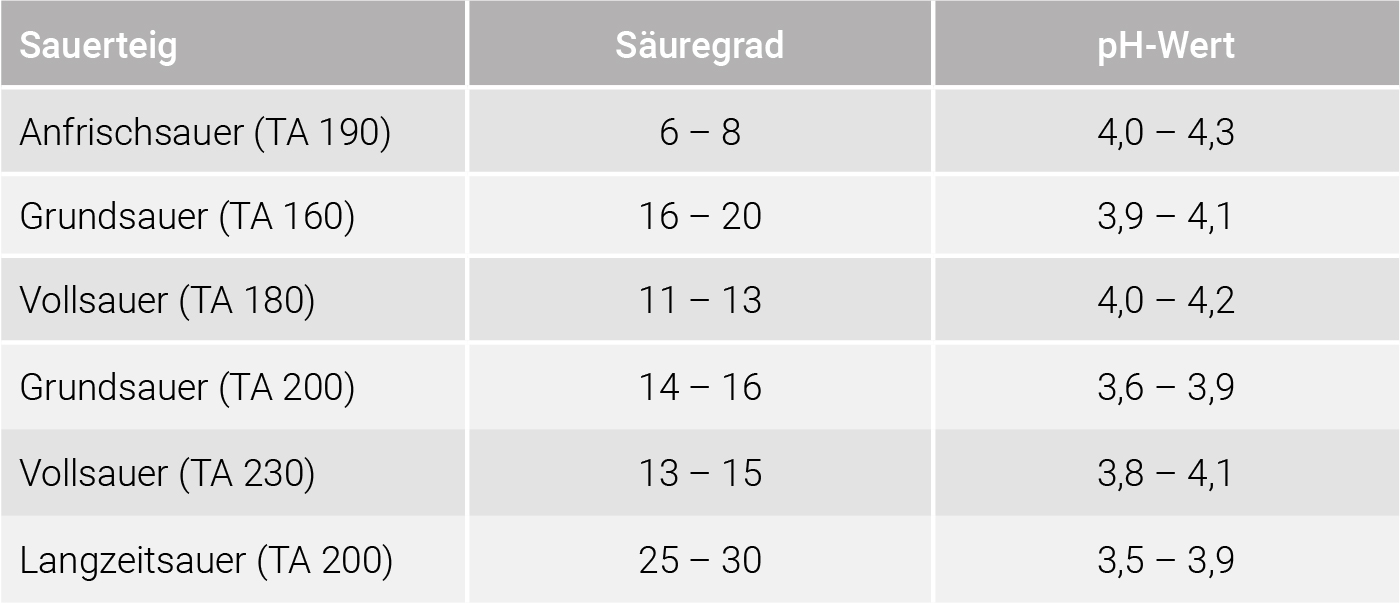
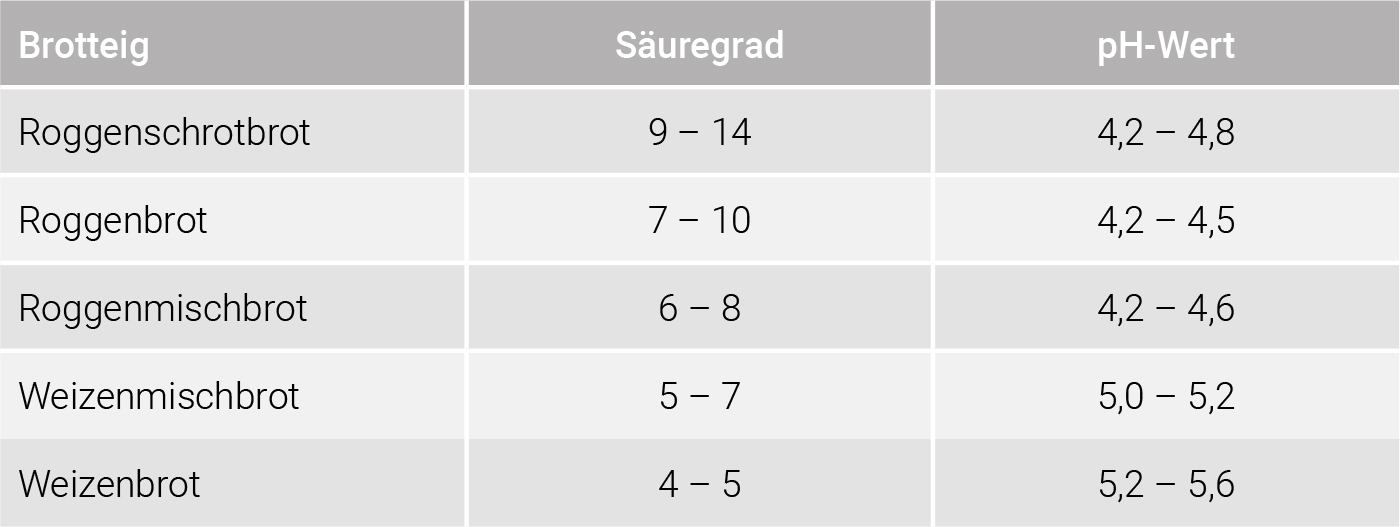
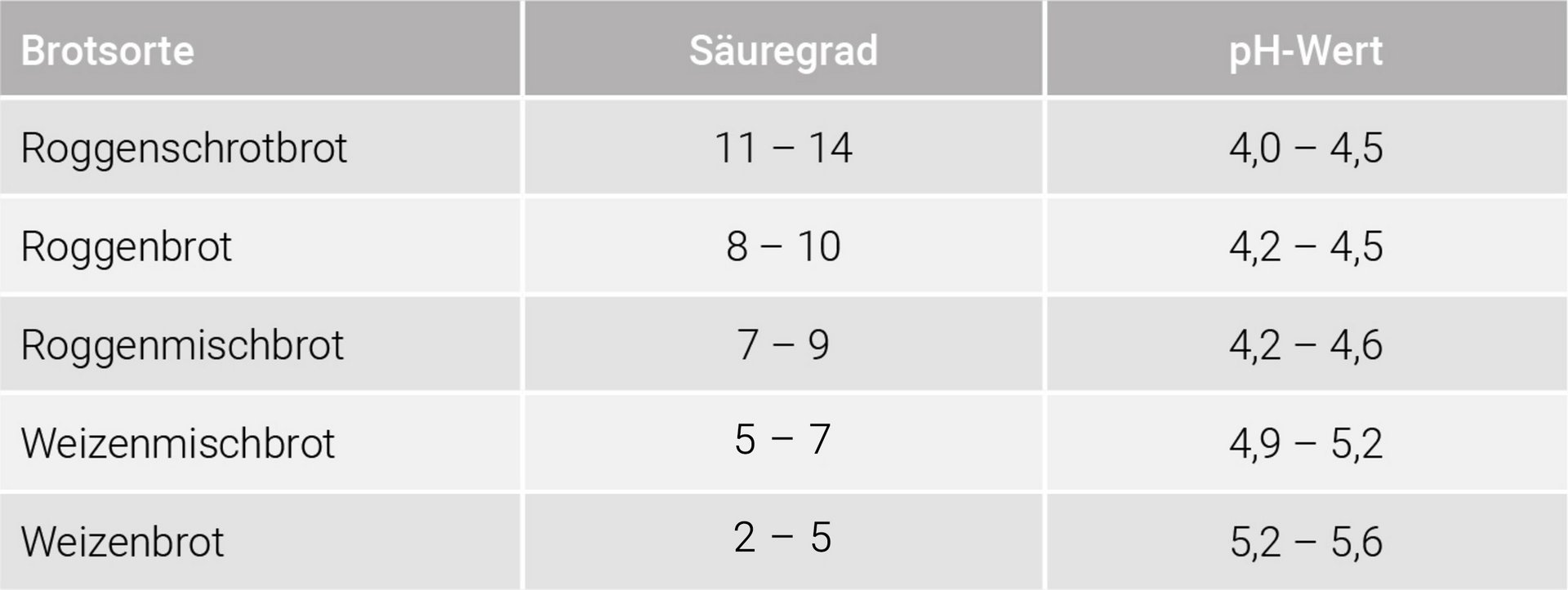
(Brand & Gänzle 2006; Meißner 2016). In den Tabellen 8.1, 8.2 und 8.3 sind Richtwerte für pH-Werte und Säuregrade verschiedener Sauerteige, Brotteige und Brotsorten dargestellt.